El injerto óseo autólogo se utiliza en diversas situaciones en ortopedia, traumatología y principalmente en reconstrucciones de cirugías ortopédicas oncológicas.
En los defectos óseos, sin duda es lo que promueve la mejor y más rápida consolidación ósea, tiene la mejor integración y la más rápida remodelación.
En segundo lugar, podemos recurrir al injerto óseo homólogo, hueso procedente de banco de tejidos, obtenido de cadáver, que tiene el inconveniente de la antigenicidad, tiene mayor tasa de infección, tarda más en incorporarse y puede producirse fragilidad estructural en el proceso de integración. Por último, podemos mencionar los productos liofilizados artificiales, que pretenden ser osteoinductivos.
Nuestro objetivo es dar a conocer la técnica que utilizamos para obtener la mayor cantidad de injerto óseo con la menor morbilidad.
Creemos que, siempre que sea posible utilizar el injerto autólogo, estaremos brindando la alternativa que permita el mejor resultado.
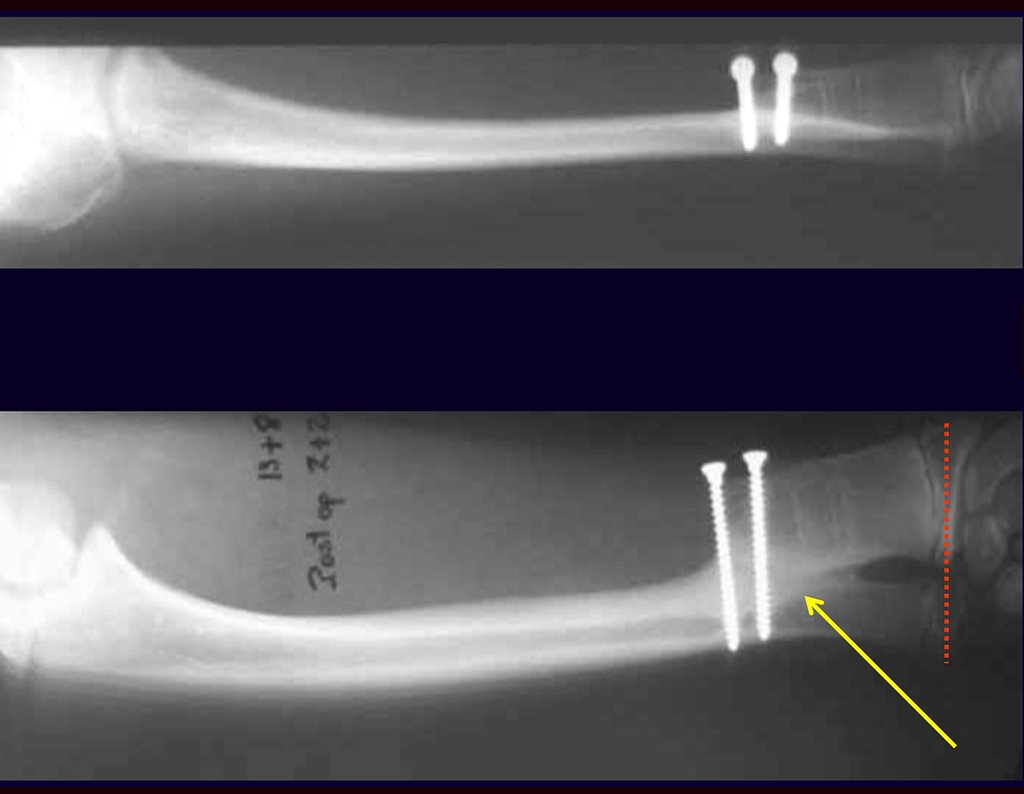
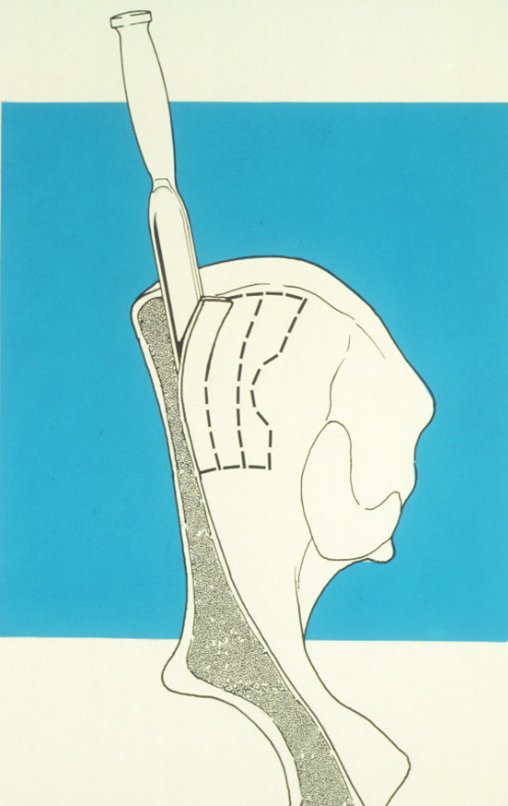
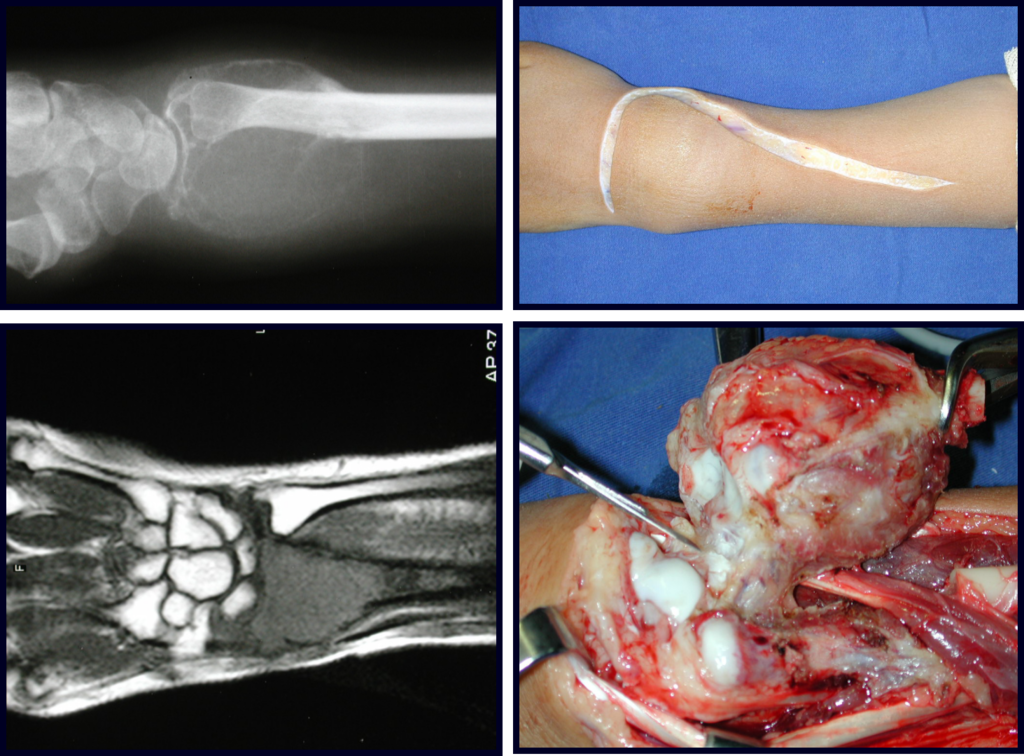
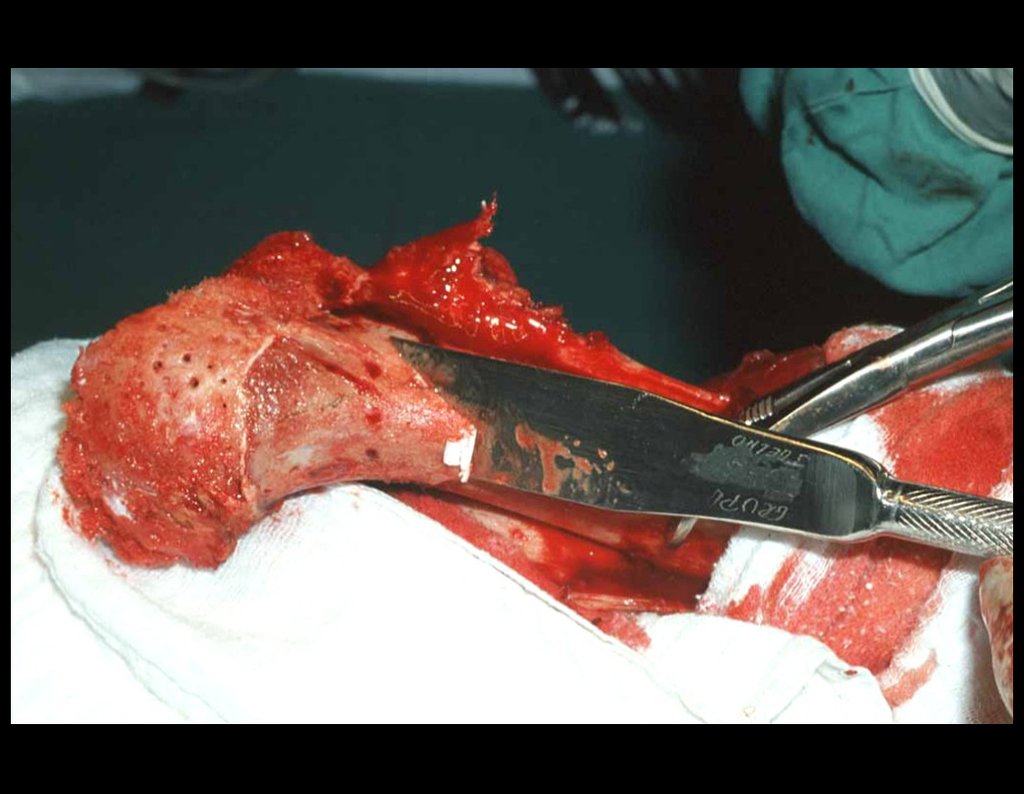
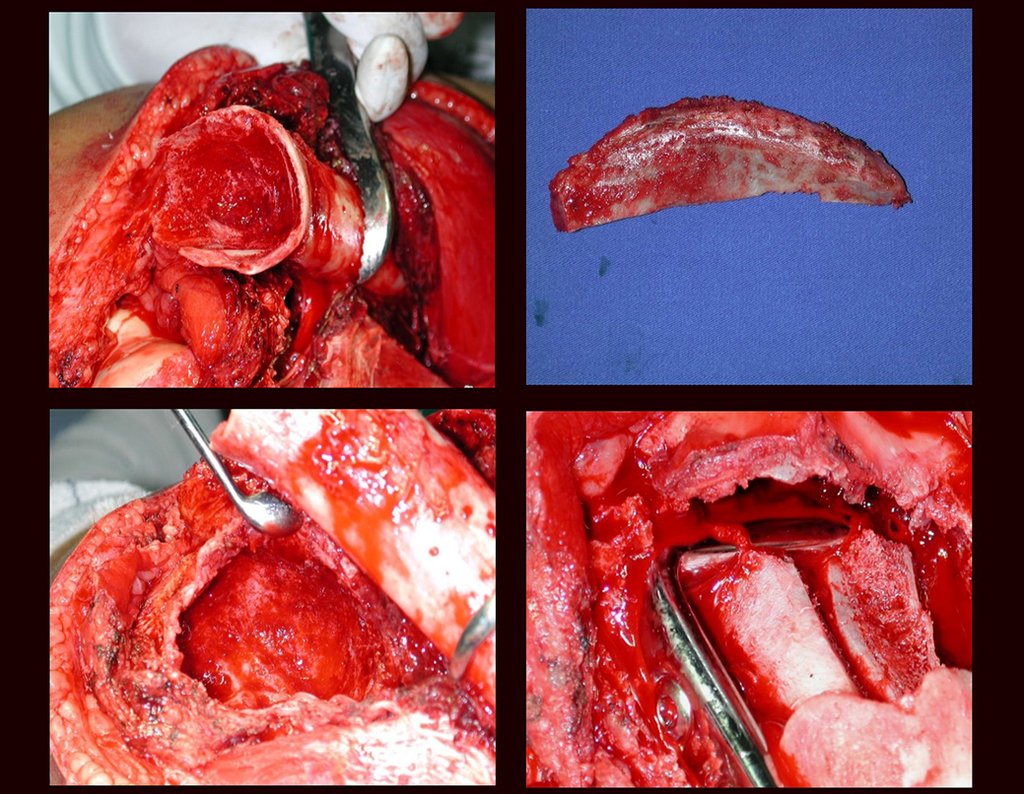
Cuando necesitamos una pequeña cantidad de injerto no cuestionamos mucho su indicación. A modo de ejemplo, en el caso de la necesidad de resecar los 3/4 proximales del radio, debido a una lesión tumoral, que pretendemos resolver realizando una “sinostosis” radiocubital distal, figuras 1 a 4.
01. Injerto óseo autólogo – Técnicas de obtención
Cuando necesitamos Reconstrucción con apertura de la sindesmosis radiocubital distal, interposición de un injerto óseo autólogo y fijación con dos tornillos Inter fragmentarios, figura 2.
Tres años después de realizar la sinostosis radiocubital distal, podemos verificar la consolidación, la integración total del injerto y observar que las fases de radio y cúbito continúan con crecimiento simétrico, con buena función, figuras 3 y 4.
La necesidad de obtener injertos en cantidad, para viabilizar grandes reconstrucciones biológicas, nos hizo mejorar la técnica quirúrgica para obtener injertos autólogos con menor morbilidad y en cantidades significativamente mayores.
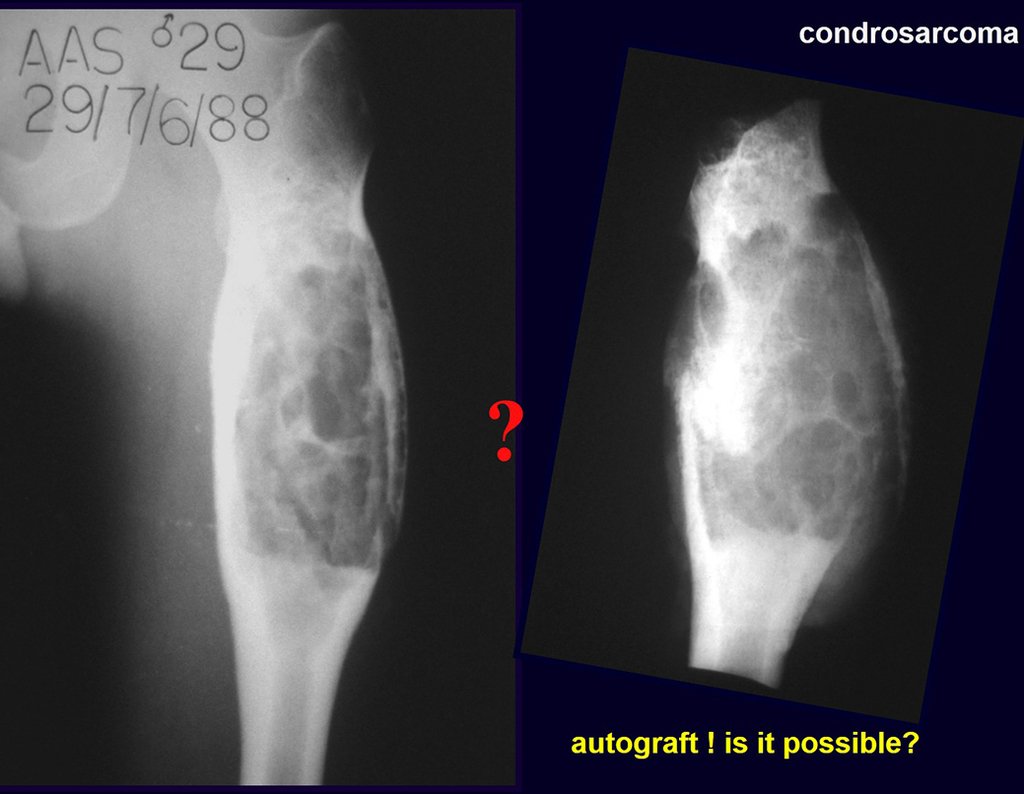
¿Es posible obtener un injerto óseo autólogo para rellenar un defecto óseo grande, de una sola placa interna de la ilíaca, como el de la figura 7? Demostremos que sí es posible, figura 8.
El injerto obtenido debe aplicarse en la reconstrucción para evitar la formación de líneas de pseudoartrosis, lo cual se explicará más adelante.
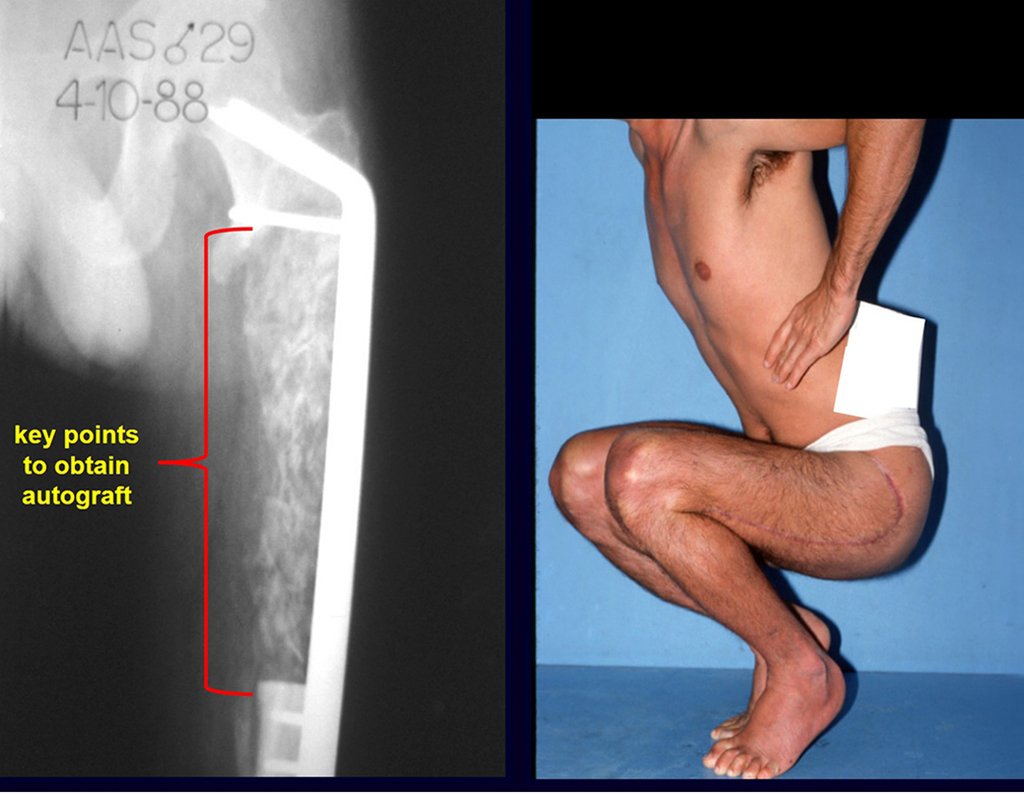
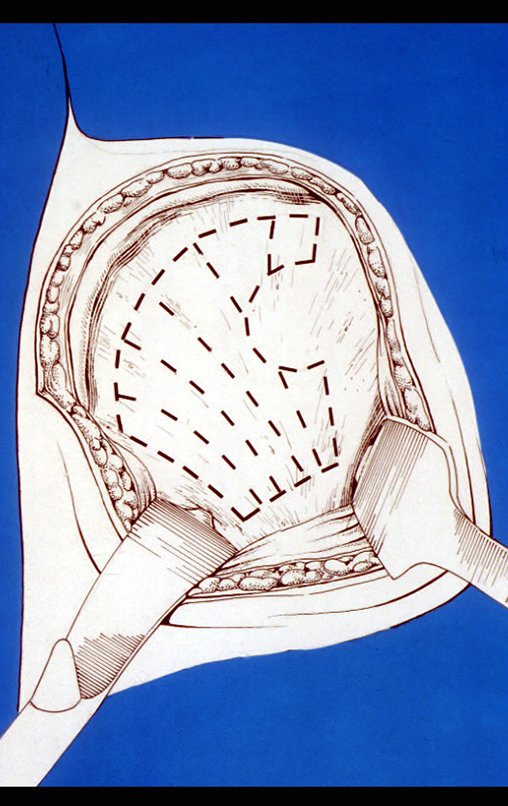
Los puntos clave y la técnica para obtener un buen injerto de hueso ilíaco se describen en
figuras. La incisión debe ser superficial, únicamente en la piel y tejido subcutáneo, para no dañar el nervio sensitivo cutáneo femoral lateral. Antes de proceder a la disección cauterizamos cuidadosamente los vasos subcutáneos con electrocauterio. figuras 9 y 10.
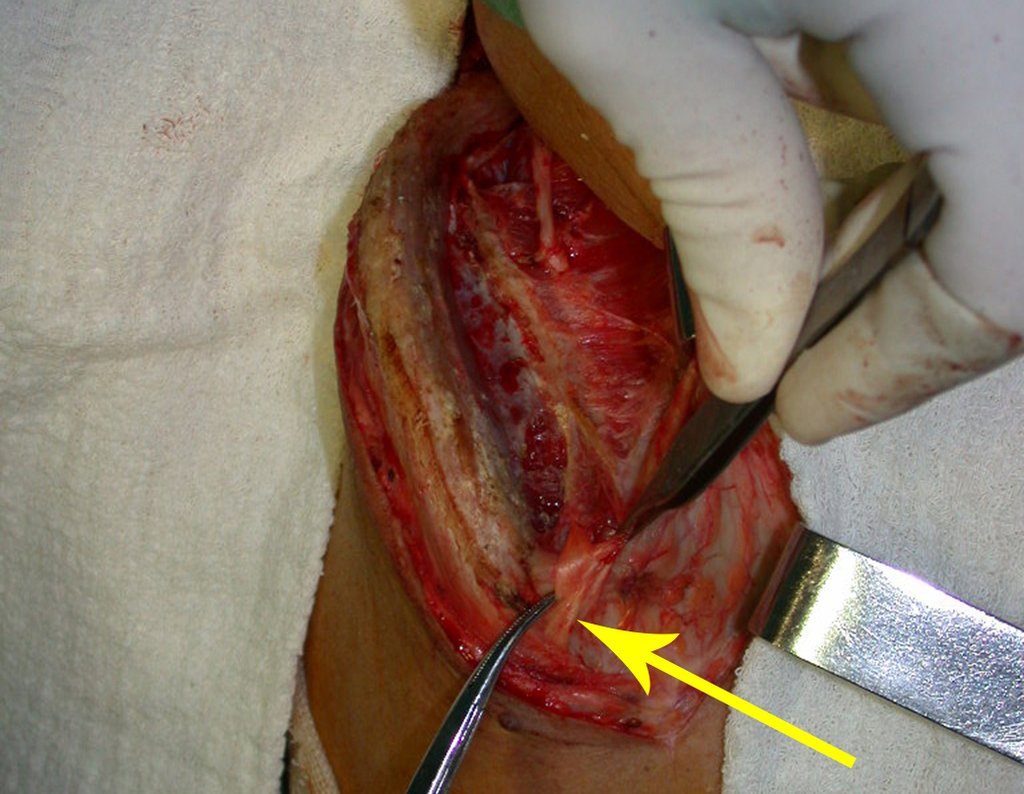
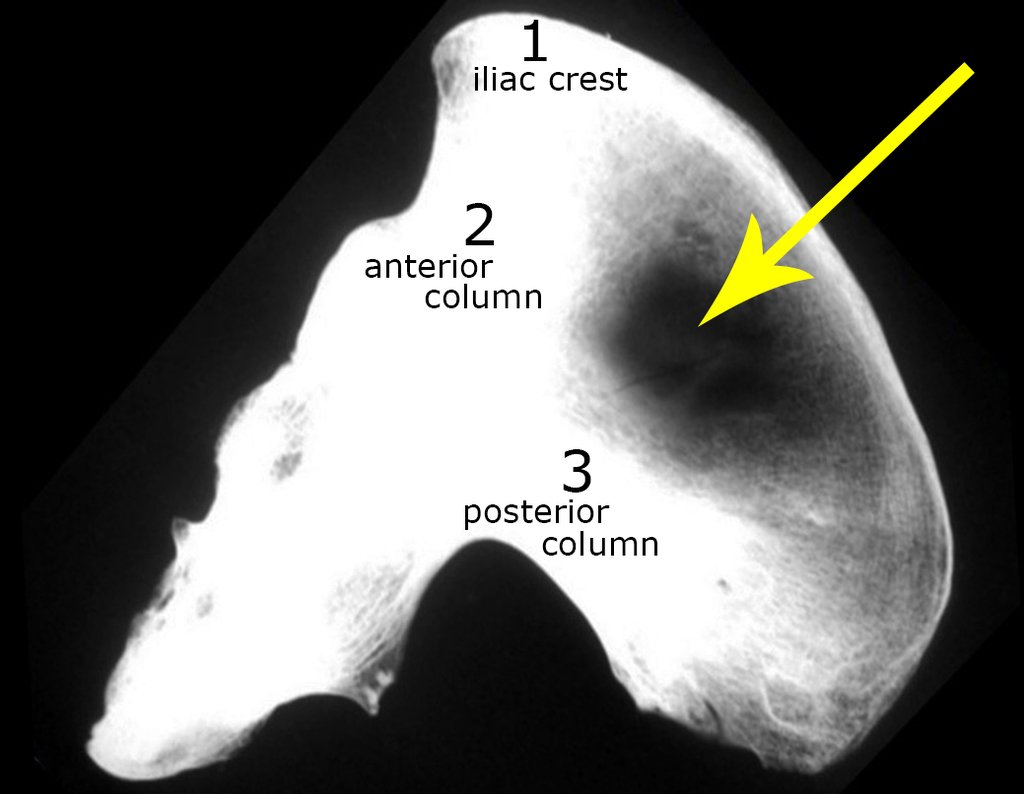
En esta etapa, con el desprendimiento del delgado periostio, se produce una gran cantidad de vasos nutritivos por los que comienza a fluir sangre. Estos deben eliminarse con hemostático de tejido óseo, con el objetivo de amortiguarlos. Debemos notar que hay una pequeña zona del hueso ilíaco donde las placas externa e interna están muy juntas, casi fusionadas. En esta pequeña “isla” no existe ningún injerto (marcado con la flecha amarilla), figura 15.
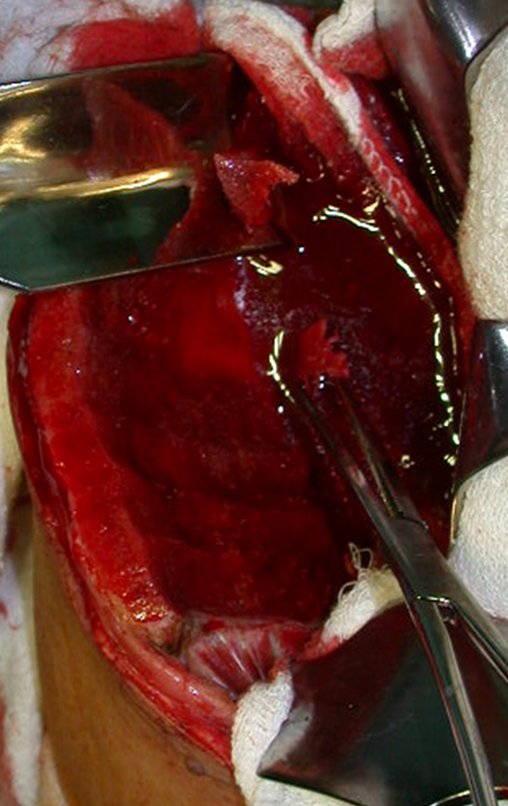
Luego de esta adecuada hemostasia, colocamos la punta de una compresa en la incisura ciática mayor y la dejamos sobre la sacroilíaca, para retener la sangre y el injerto. Comenzamos con un osteótomo para extirpar la corteza superior de la cresta ilíaca. Debemos iniciar la retirada del injerto con hemostasia controlada, figura 16.
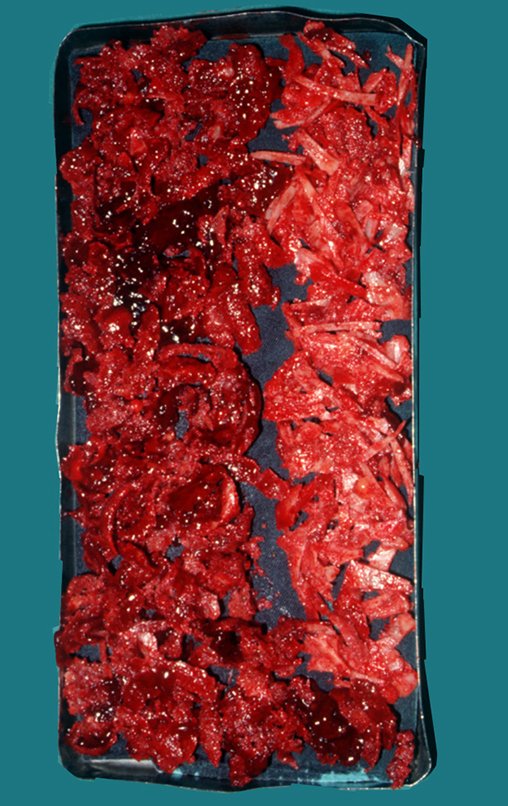
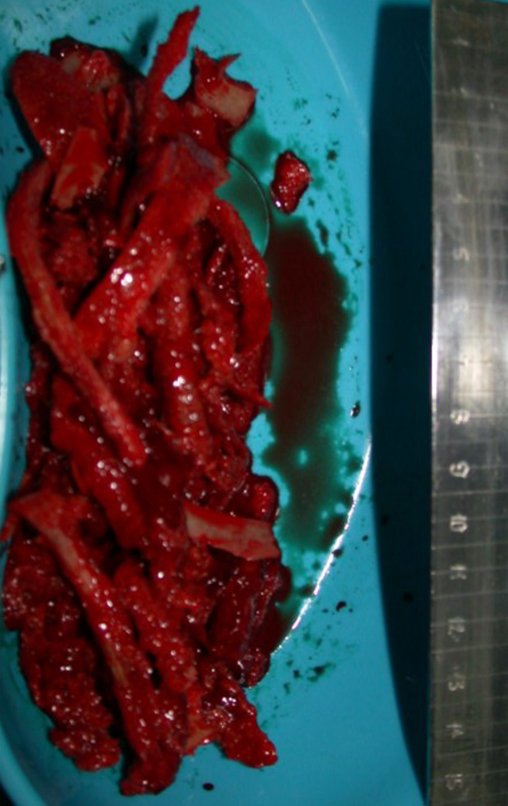
Después de retirar toda la corteza interna, guardamos el injerto en una tina, empapado del coágulo recogido, preservando así las células totipotentes, que también se colocarán en el defecto óseo. A continuación, con un cincel afilado y SIN utilizar martillo, procedemos a la extracción del hueso ilíaco esponjoso, figuras 20 a 23.
Cuando es necesario colocar al paciente en decúbito prono, como en las cirugías de columna, podemos obtener más fácilmente un injerto autólogo, dejando expuesto el hueso ilíaco.
En este abordaje, la mejor incisión es horizontal, al nivel de la espina ilíaca posterosuperior. Esta incisión es más estética y puede ocultarse fácilmente con un bikini, además de facilitar tanto la exposición de la cresta ilíaca como de la columna posterior, figuras 30 y 31.
Es importante recordar el concepto de reparación de defectos óseos con injertos óseos: EN UNA RECONSTRUCCIÓN BIOLÓGICA, TODO INJERTO ÓSEO COLOCADO PARA LLENAR CAVIDADES O FALTAS SEGMENTALES PASA POR UNA FASE DE REABORTO PARA POSTERIOR REINTEGRARSE , REPARANDO LA PÉRDIDA ÓSEA. El injerto debe estar entrelazado y sobrepasar el nivel de la osteotomía, evitando pseudoartrosis, como ejemplifica este caso de condrosarcoma en las figuras 36 a 38, flechas azules.
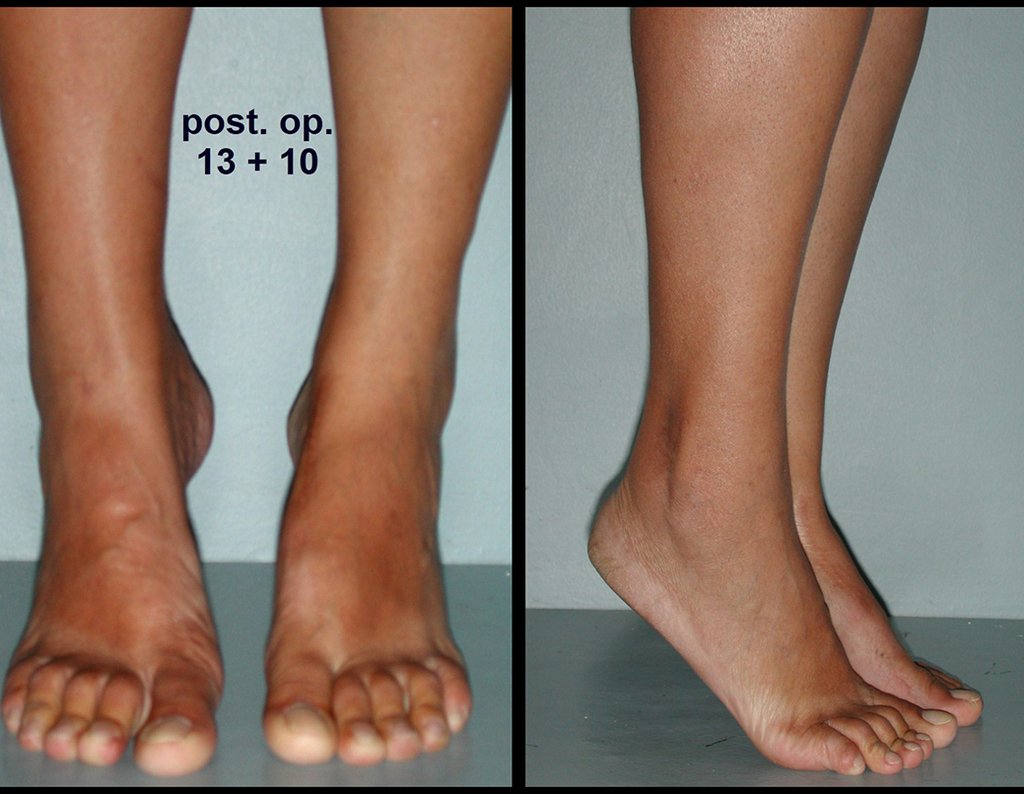
Video 3: Buena estética y función, 22 años después de la cirugía.
Este caso puede verse completo accediendo al enlace: http://bit.ly/sarcoma-de-Ewing
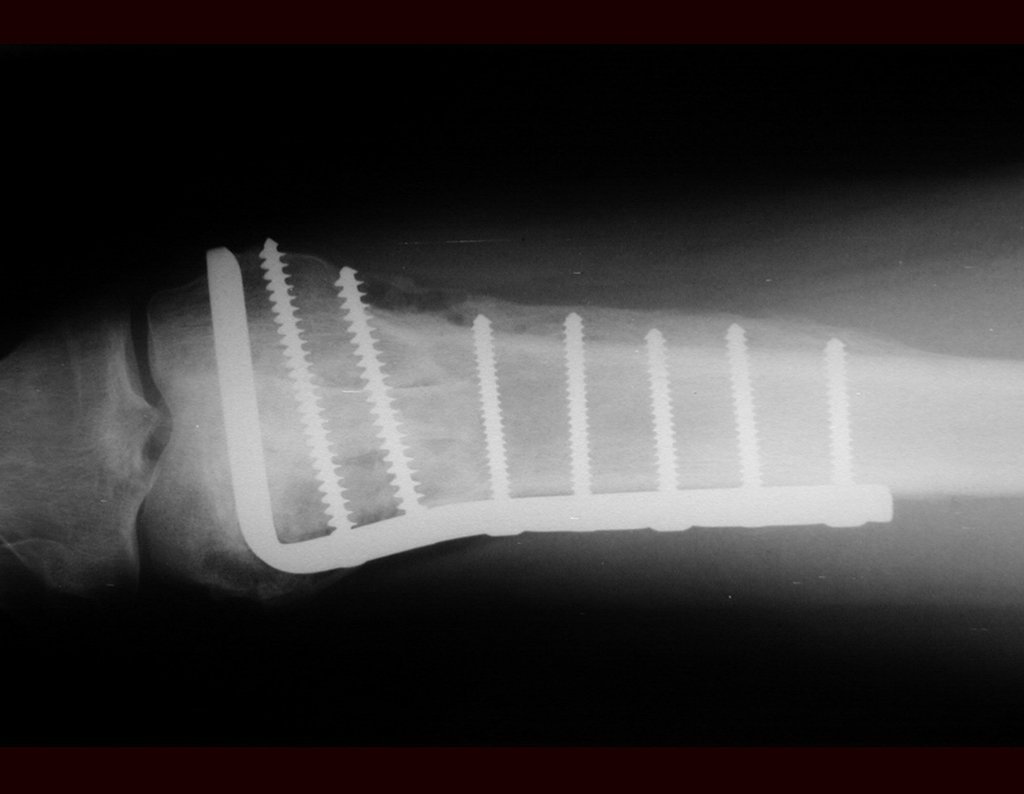
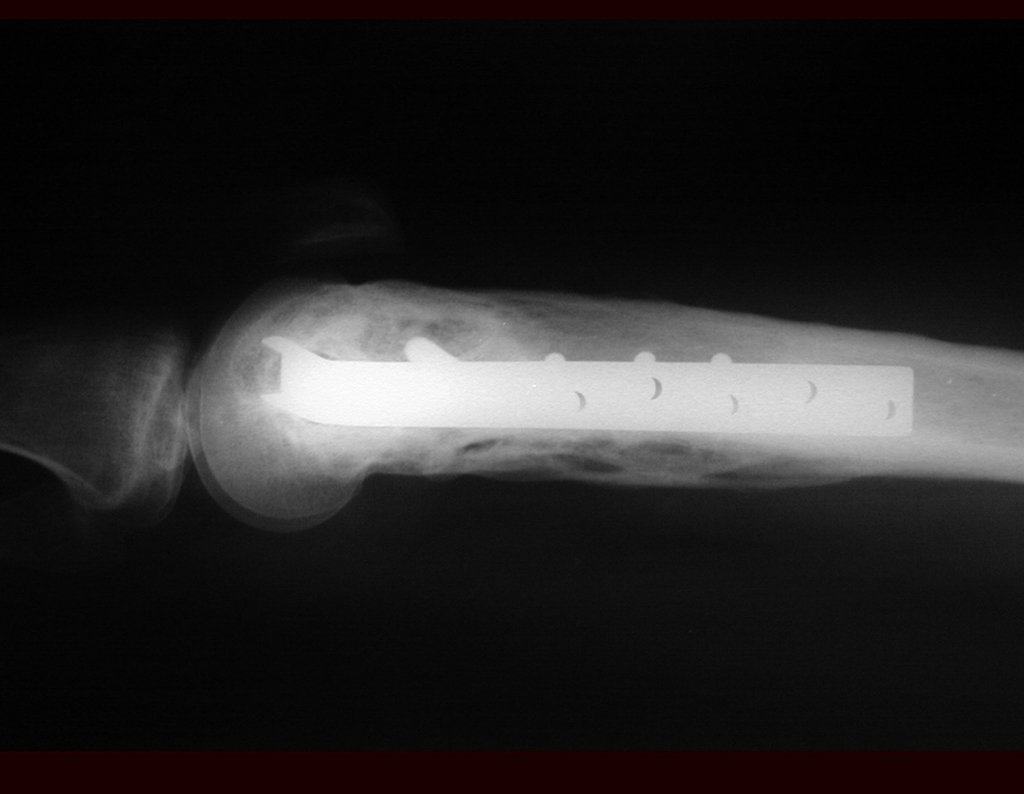
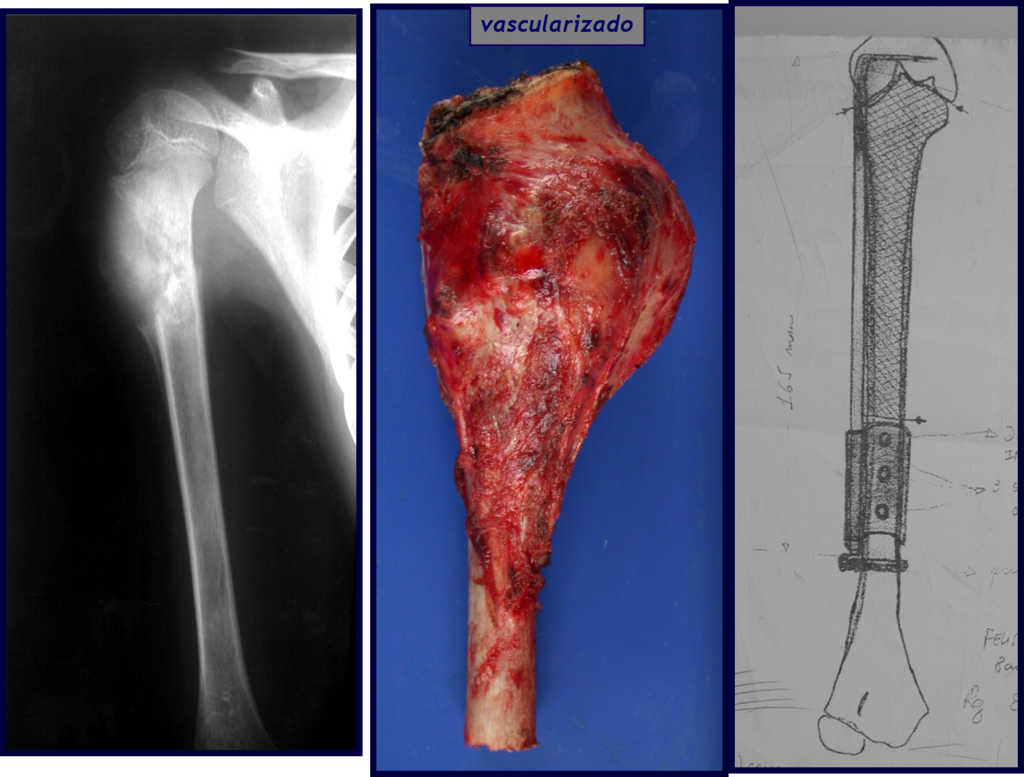
El peroné también se puede utilizar vascularizado en reconstrucciones, incluso con la placa de crecimiento para reemplazar la que será resecada debido al tumor. Se trata de un autotrasplante de peroné con la placa fisaria, realizándose osteosíntesis con el dispositivo de fijación interna extensible, figuras 63 y 64.
En la reconstrucción de pequeños segmentos, como en la reconstrucción del radio, por traumatismos o tumores, podemos utilizar el peroné libre con buenos resultados, figuras 65 y 66.
Este caso puede verse completo accediendo al enlace: http://bit.ly/tgc_radio
Autor: Profr. Dr. Pedro Péricles Ribeiro Baptista
Oncocirugía Ortopédica en el Instituto Oncológico Dr. Arnaldo Vieira de Carvalho
Oficina : Rua General Jardim, 846 – Cj 41 – Cep: 01223-010 Higienópolis São Paulo – SP
Teléfono: +55 11 3231-4638 Celular:+55 11 99863-5577 Correo electrónico: drpprb@gmail.com