¡¿Condrosarcoma o condroma?!: Diagnóstico diferencial, manejo y tratamiento. Reconstrucción del Húmero con Endoprótesis.
¿Condrosarcoma o condroma? Para comprender mejor el diagnóstico diferencial entre condroma y condrosarcoma grado I, analicemos el caso:
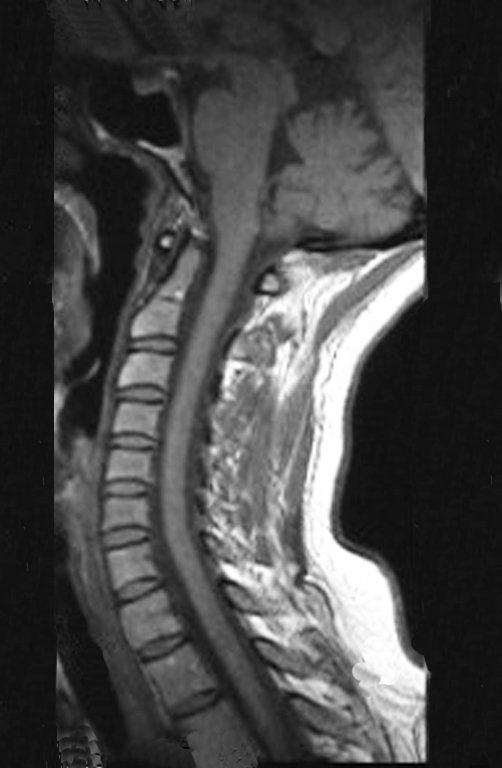
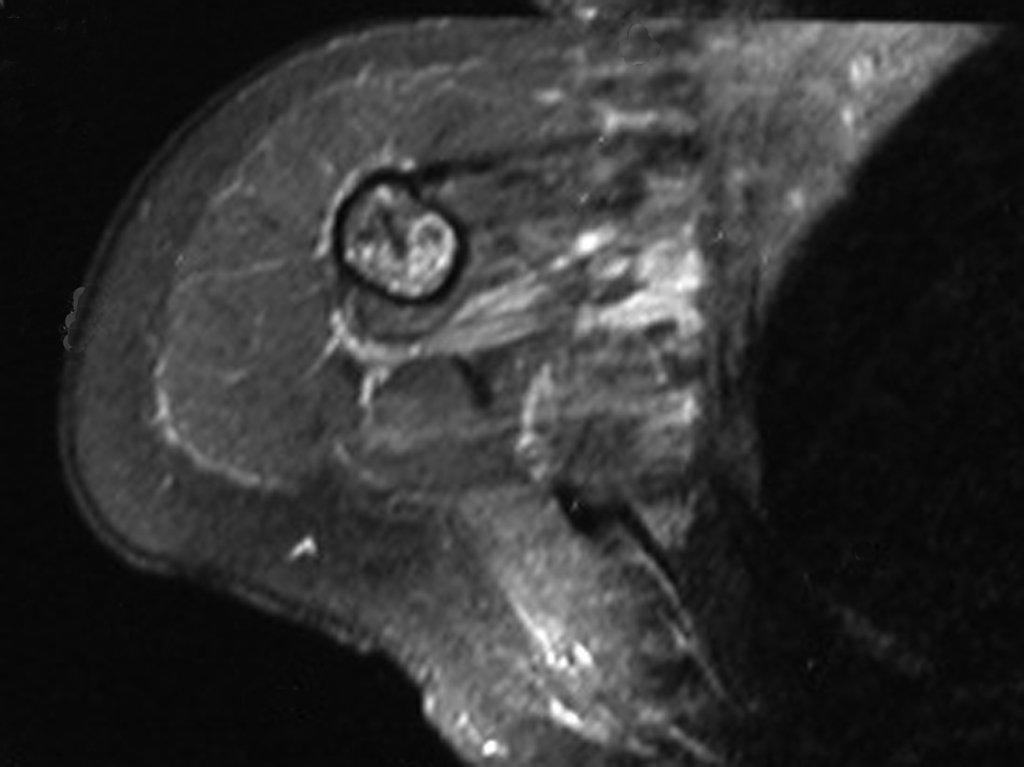
Paciente mujer, 39 años, dentista, diestra, refiere dolor en el hombro derecho desde hace ocho meses. El primer médico realiza radiografías de la columna cervical y aconseja fisioterapia para la cervicobraquialgia (Figura 1). Al no haber mejoría se realizó resonancia magnética de columna, la cual no mostró cambios cervicales (Figura 2).
La radiografía de esta región, realizada el 24 de julio de 2003, dos semanas después, destacó la presencia de esta lesión metadiafisaria, ocupando dos tercios del extremo proximal del húmero.
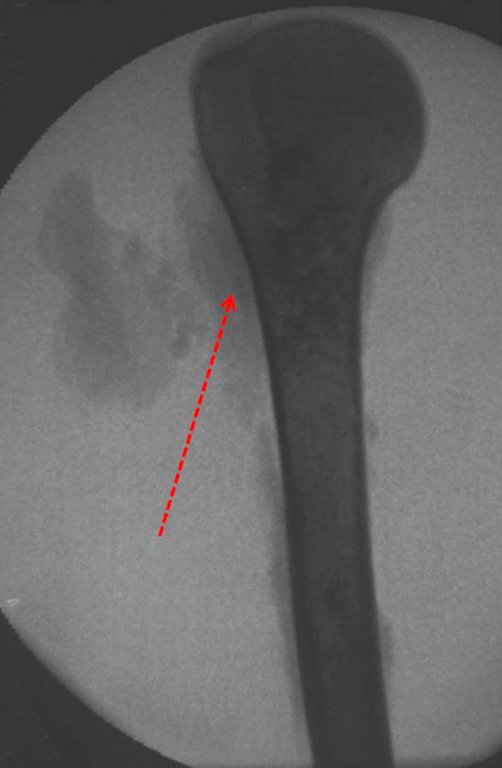
Esta imagen muestra áreas de rarefacción en “bolsa de mordedura”, agrandamiento de la médula ósea, debido a erosión de la corteza interna y áreas de condensación moteadas, con apariencia algodonosa, sugiriendo focos de calcificación (Figura 6.A).
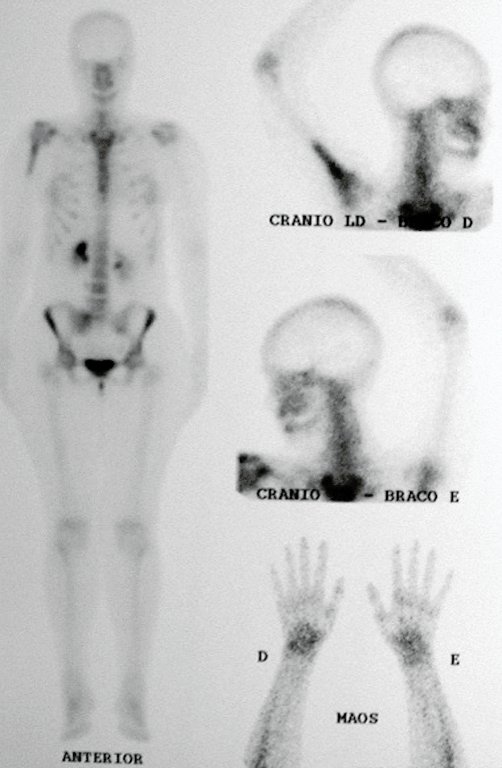
Tras este hallazgo, fue derivada a un oncólogo, quien solicitó pruebas para investigar y estadificar la lesión. En la gammagrafía realizada se observó hipercaptación únicamente en el húmero derecho (Figura 6.B).
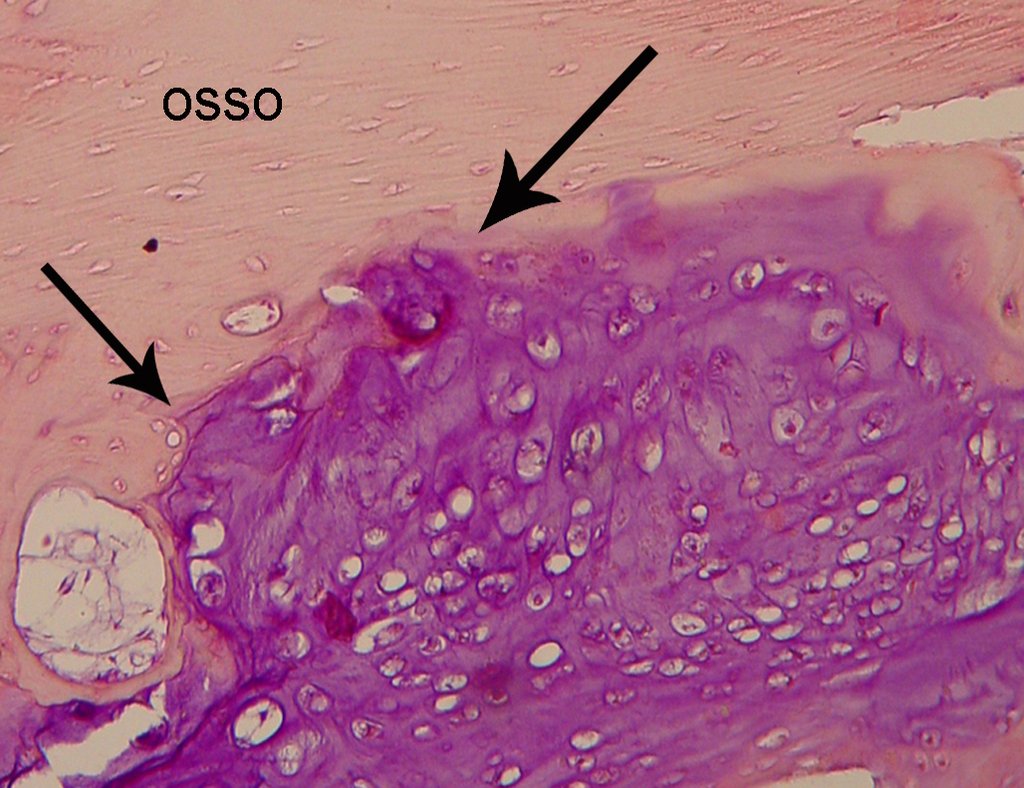
Seguidamente se realizó biopsia de húmero, que reveló tejido cartilaginoso, sin atipia, sugiriendo una nueva biopsia (Figura 7).
Con el cuadro clínico de dolor en el hombro y los hallazgos imagenológicos de una lesión agresiva, con focos de calcificación, se planteó la hipótesis de condrosarcoma. En esta ocasión, el diagnóstico diferencial del condroma y, más remotamente, del infarto óseo debe descartarse por las siguientes consideraciones:
1- La paciente acudió al médico por dolor progresivo, no fue un hallazgo casual en la exploración.
2- La radiografía muestra agrandamiento metafisario, erosión de la corteza interna y focos de calcificación, lo que combinado con el cuadro clínico indica que se trata de una lesión activa, con agresividad local y apunta al diagnóstico de condrosarcoma.
3- Los apartados de resonancia magnética complementan los datos de la imagen y despiertan el razonamiento, cerrando el mismo diagnóstico.
4- La biopsia reveló que se trataba de “tejido cartilaginoso”, no tiene lógica sugerir una nueva biopsia en esta situación.
La biopsia en este caso es académica porque el diagnóstico histopatológico entre condroma y condrosarcoma grado I suele ser difícil, y el tratamiento en este caso es quirúrgico. Como sabemos que la cirugía es el único tratamiento que puede curar el condrosarcoma, este caso debe ser abordado y tratado quirúrgicamente como un condrosarcoma, independientemente de que la eventual biopsia venga con un diagnóstico previo de condrosarcoma. Puede estar indicada una biopsia sólo para confirmar que se trata de una lesión cartilaginosa.
El primer médico decidió realizar una biopsia utilizando una aguja JamShidi. El resultado del examen anatomopatológico fue una lesión cartilaginosa sin atipia. Preocupado por la imagen agresiva de la lesión, no se sentía cómodo tratando el caso como un condroma ni dando el paso de tratarlo como un condrosarcoma. Propuso que el paciente estuviera en observación durante dos meses.
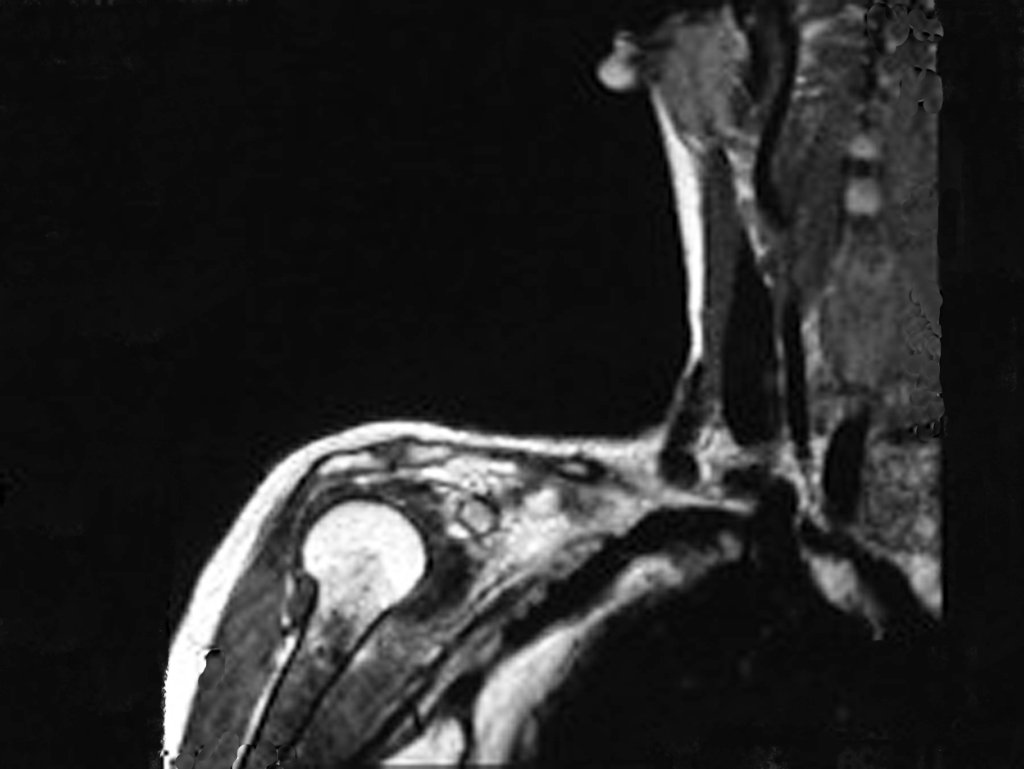
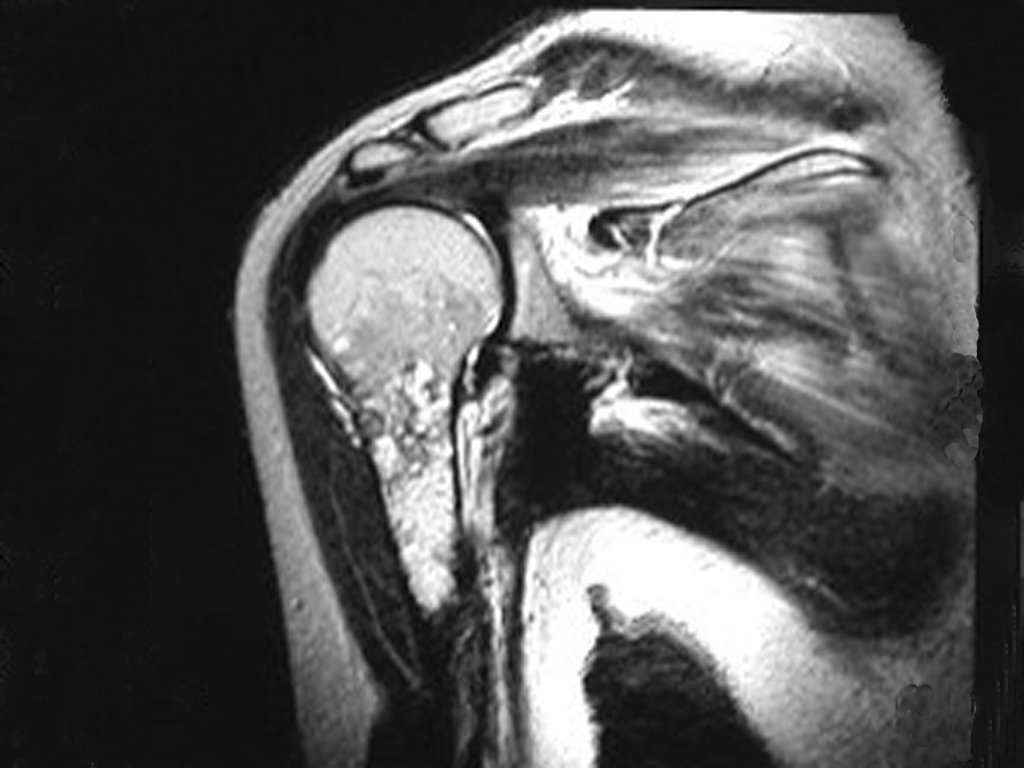
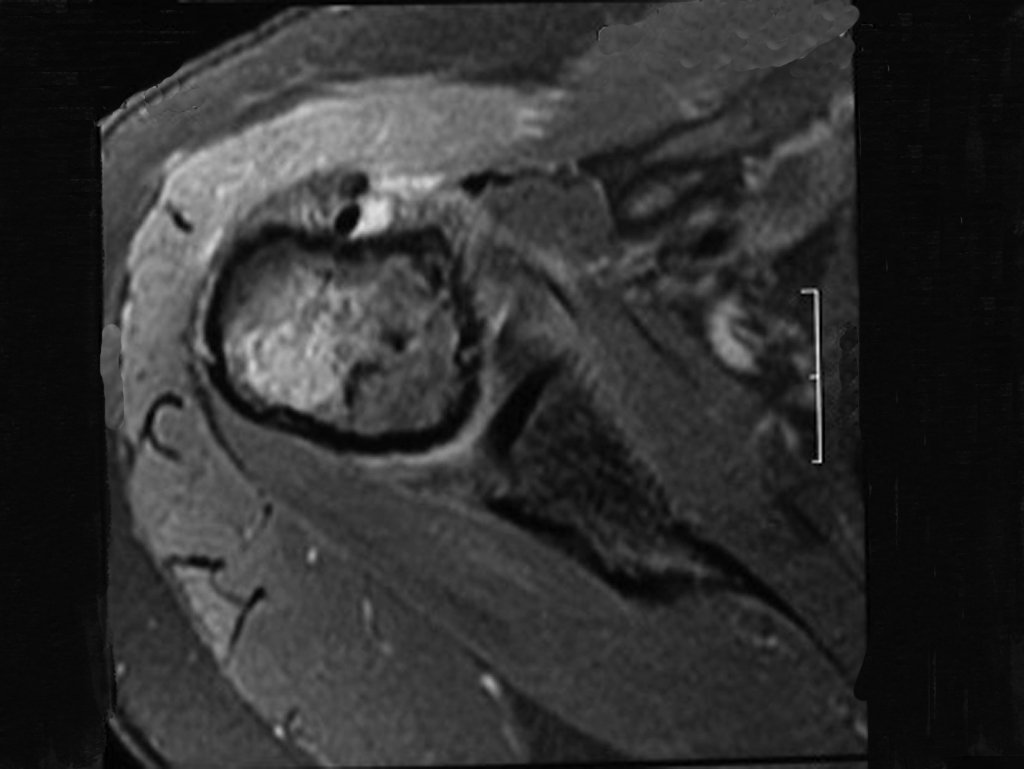
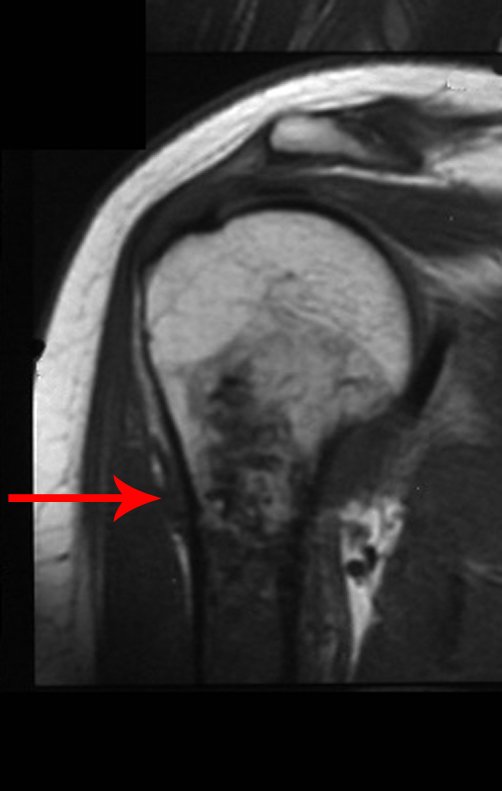
Pasado este período, el paciente regresa, aún con el mismo cuadro clínico. El médico solicita una nueva resonancia, observando los mismos aspectos que antes, la cicatriz de la biopsia y la presencia ahora de un tumor extracortical, contaminando todo el tejido subcutáneo (Figuras 8.A, 8.B, 8.C y 9).
Después de este último examen, el médico le sugerirá realizar una nueva biopsia. El paciente decide consultar a otro profesional, busca una segunda opinión y acude a nosotros.
El especialista en oncología ortopédica debe completar el diagnóstico y definir el curso de acción en este momento. No se debe realizar una nueva biopsia, ya que ¿qué acción se tomará si esta biopsia no es concluyente para condrosarcoma? ¿Qué hacer si llega el condroma?
Con los datos clínicos que revelaron dolor progresivo, exámenes de imagen con una lesión localmente agresiva e incluso el análisis anatomopatológico de una lesión cartilaginosa, el especialista tiene todos los parámetros para indicar el tratamiento de esta lesión como condrosarcoma, como el diagnóstico histopatológico entre condroma y condrosarcoma. El grado I es muy difícil y en ocasiones controvertido (Figuras 10 y 11).
La misma diapositiva, presentada al mismo patólogo, después de algún tiempo, puede cambiar el informe de condroma a condrosarcoma de grado I, o de condrosarcoma de grado I a condroma. Además, si se presenta esta misma diapositiva a otros patólogos, podemos obtener los dos diagnósticos diferentes. Sabemos que el diagnóstico final de los tumores óseos debe tener correlación CLÍNICA-RADIOLÓGICA y ANATOMOPATOLÓGICA. Por lo general, el patólogo solo analiza el portaobjetos. Quien lleva el caso es quien tiene todos los datos. Hay que valorar, por tanto, los exámenes de imagen y todo el cuadro clínico ante esta situación.
Tras estas consideraciones, es necesario el tratamiento quirúrgico. El condrosarcoma no responde a la quimioterapia ni a la radioterapia. Se puede curar con resección quirúrgica, con margen oncológico, ya que lamentablemente recurre localmente cuando no se obtiene este margen. En la recurrencia puede ocurrir desdiferenciación e invasión de tejidos adyacentes, lo que complica o impide la cirugía de rescate del miembro, además de posibilitar la aparición de metástasis.
No se puede perder la oportunidad de curar esta lesión con una cirugía adecuada.
Un análisis cuidadoso de las imágenes en este caso indica la necesidad de una resección amplia, con márgenes y reemplazo por una prótesis no convencional.
El legrado intralesional está contraindicado, incluso con adyuvante local y relleno de cemento, ya que la recurrencia y la desdiferenciación son frecuentes con este abordaje.
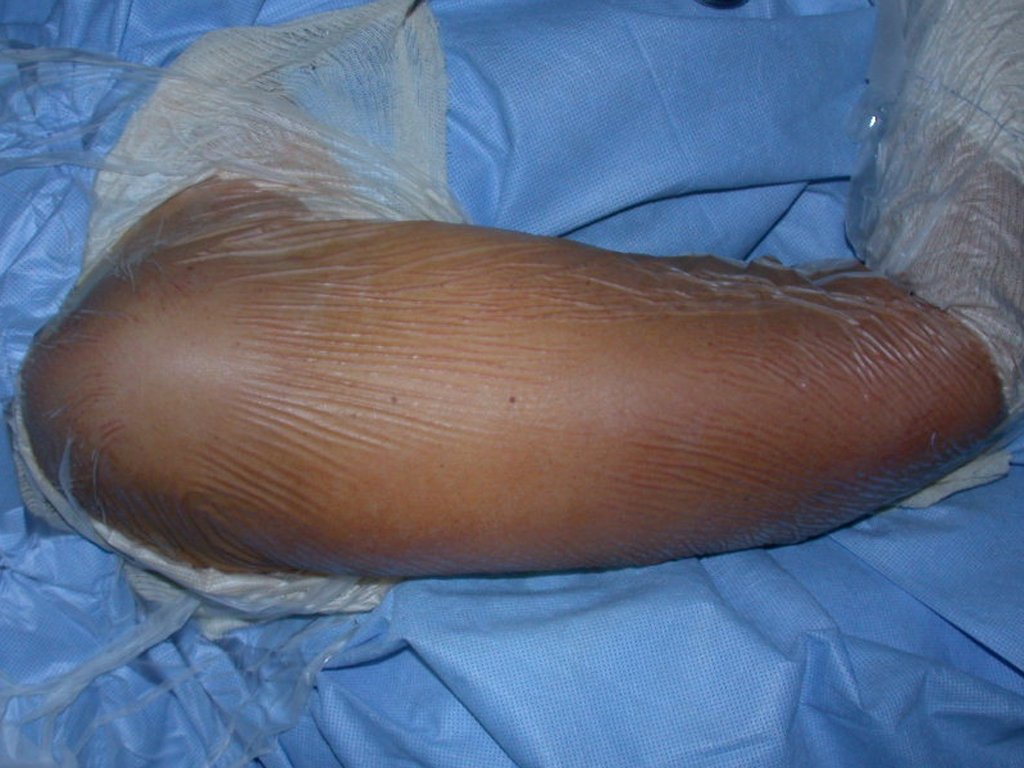
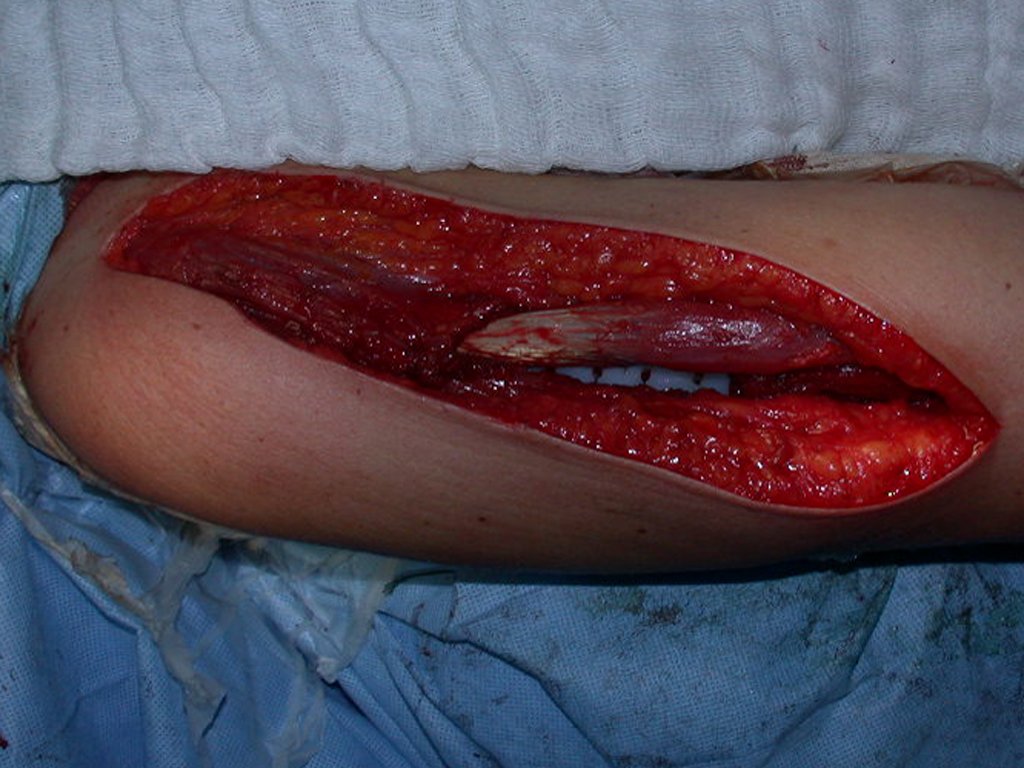
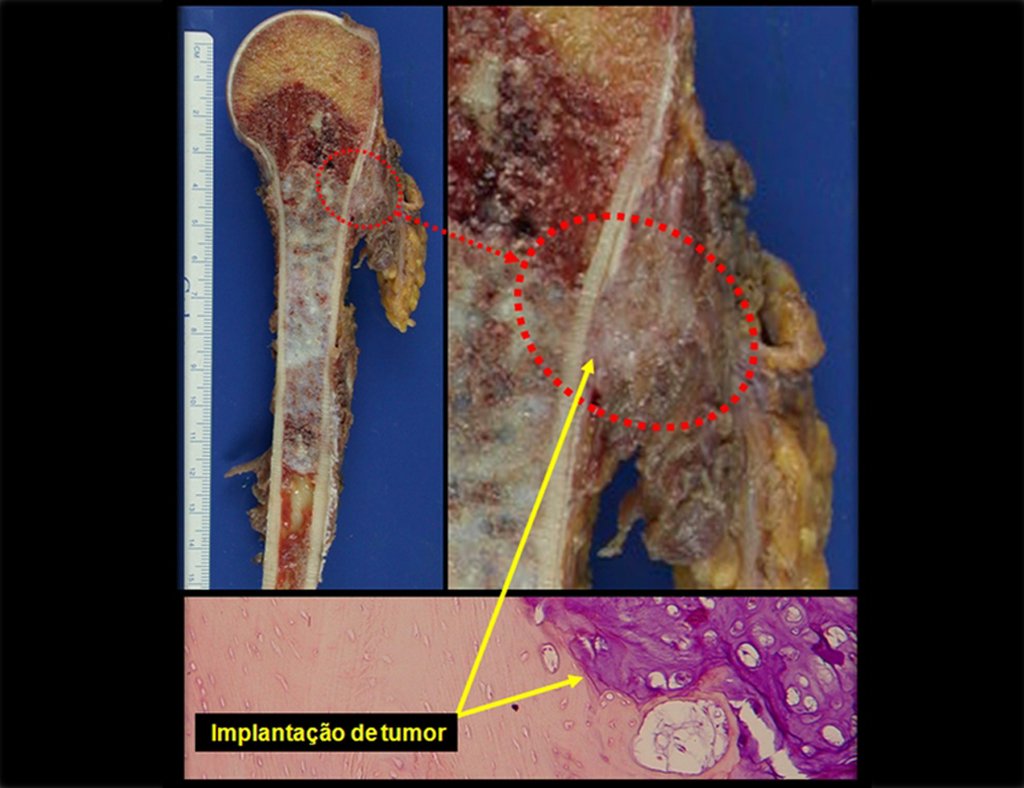
Tras esta aclaración al paciente, realizamos cirugía de resección de los dos tercios proximales del húmero, incluyendo la piel y el trayecto de la biopsia, ya que, además de que el condrosarcoma podía implantarse en los tejidos blandos, en este caso ya estaba ocurriendo. a través del camino de la biopsia.
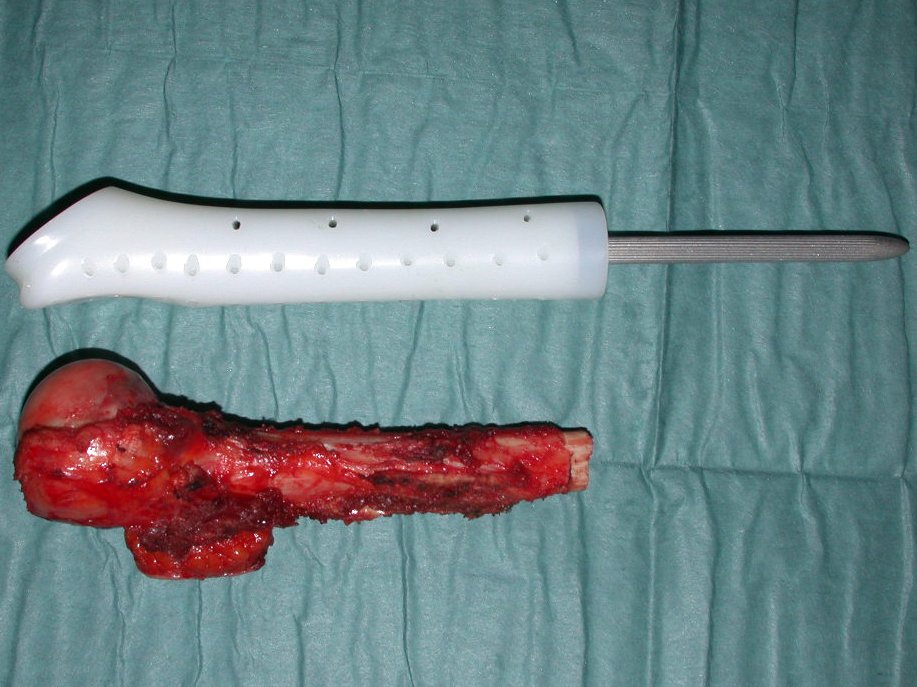
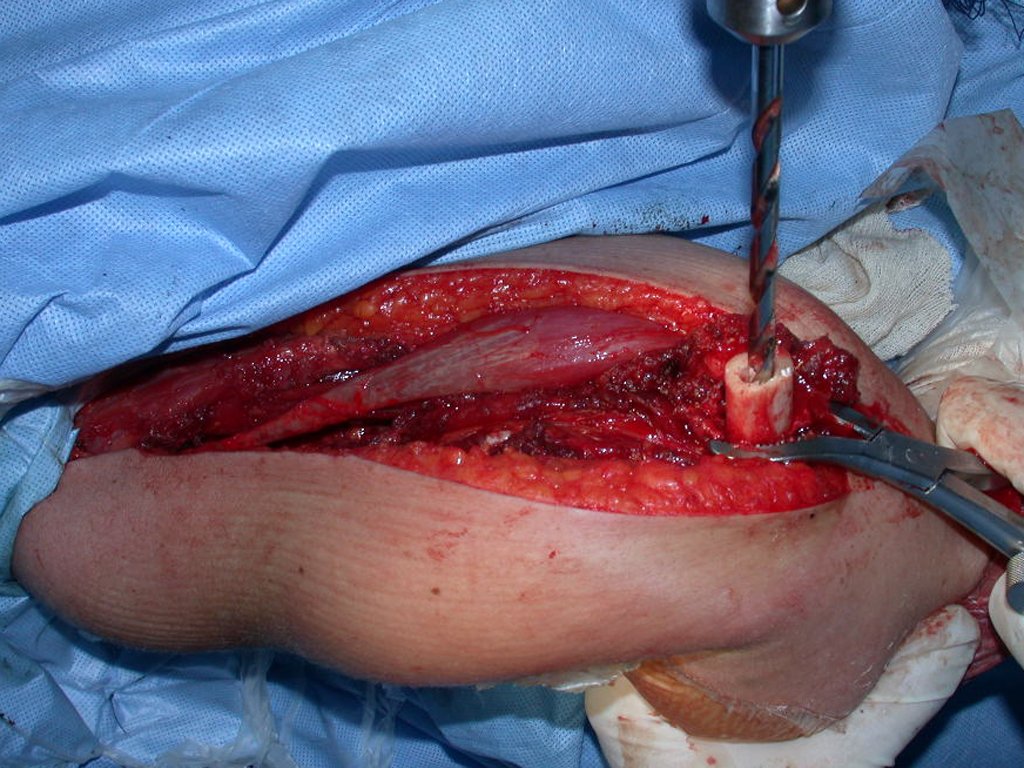
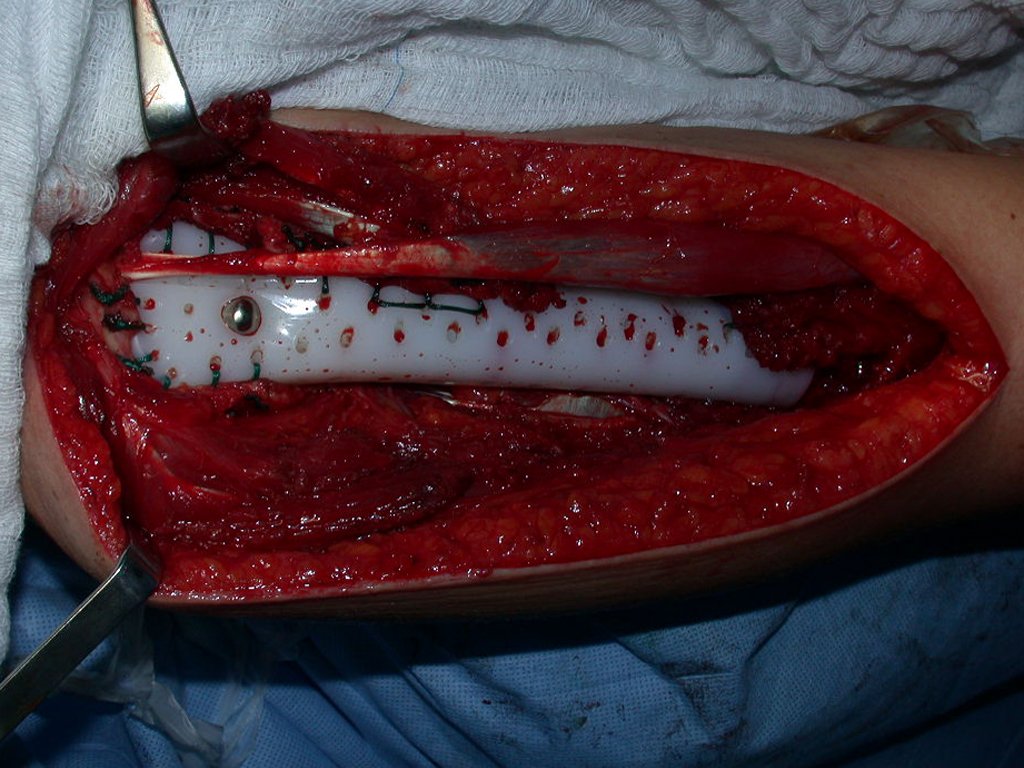
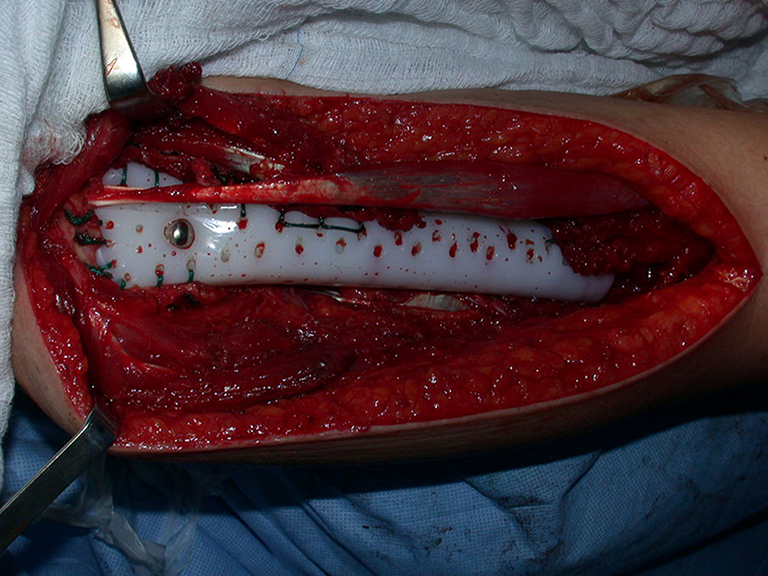
Para reconstruir el húmero utilizamos endoprótesis de polietileno no convencionales. Son más ligeros que los metálicos, tienen una elasticidad similar a la de los huesos y permiten realizar agujeros, cuando sea necesario, para reinsertar los ligamentos y músculos restantes. Se produce una reacción fibrótica alrededor del polietileno, que involucra la prótesis y fija definitivamente los tejidos blandos reinsertados.
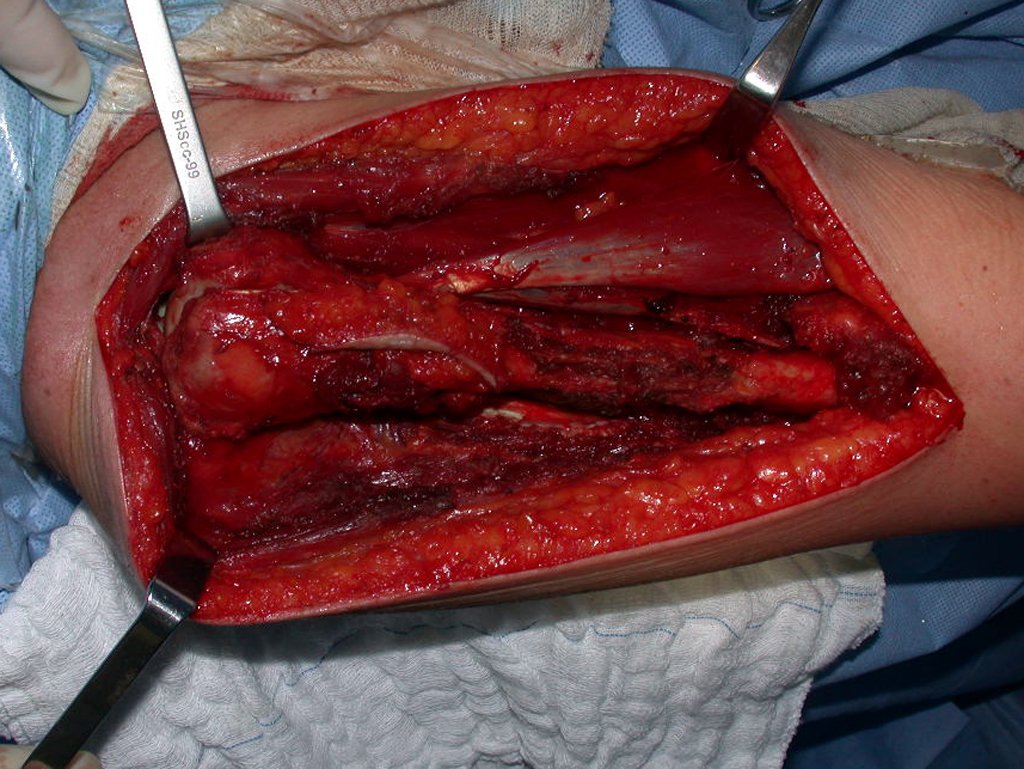
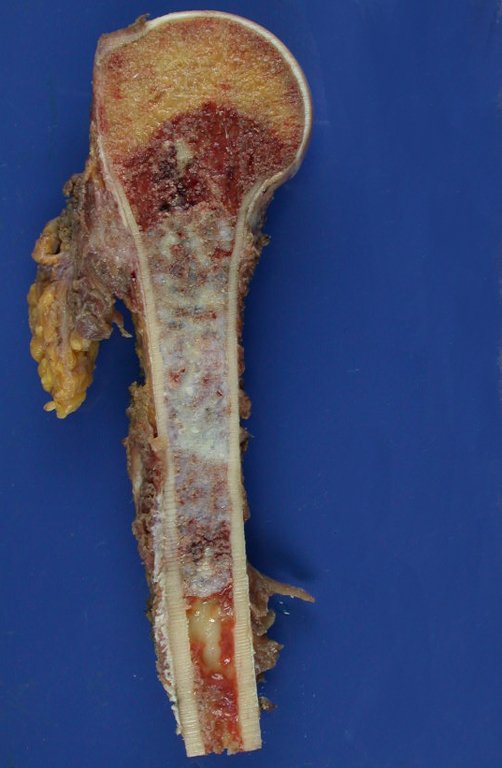
En detalle presentamos los pasos de la cirugía, la reconstrucción con la endoprótesis y la anatomía patológica de la pieza (figuras 12 a 23).
La cirugía oncológica debe buscar primero la resección, buscando obtener márgenes que reduzcan la posibilidad de recidiva local. Una vez logrado este objetivo, se debe realizar la mejor reconstrucción para restaurar la función al punto más cercano a la normalidad. En las endoprótesis no convencionales, realizadas para reconstruir resecciones tumorales, no podemos esperar la misma función que las prótesis convencionales, utilizadas en artrosis o en otras indicaciones, ya que en cada caso tendremos una pérdida mayor o menor de músculos y tejidos blandos sanos. resecado por necesidad de obtención de margen oncológico.
La fisioterapia guiada por un profesional que conoce la cirugía es fundamental para conseguir un buen resultado funcional (figuras 24 a 27).
REVISIÓN:
El condrosarcoma es el tumor óseo maligno primario más común después del osteosarcoma 23,24) . El subtipo central es el más común y afecta cinco veces más que el subtipo periférico (3) , siendo raros los subtipos de células claras y mesenquimatoso (2) .
El condrosarcoma de grado I no produce metástasis y se denomina sarcoma porque es de naturaleza mesenquimatosa, a diferencia del cáncer, que se deriva del tejido ectodérmico. Es el tercer tumor óseo más común después del osteosarcoma y el de Ewing.
Normalmente aparece en huesos de origen endocondral y principalmente en las raíces de las extremidades (hombro, pelvis, costilla y esqueleto axial (1) ) y es rara en los de origen membranoso (24,11,15,14) . Es de crecimiento lento y el paciente suele buscar tratamiento cuando la lesión es grande. Este tumor puede afectar a cualquier edad, con predominio entre los 30 y 40 años (7, 11, 22) , existiendo referencias en la literatura desde los tres años (15) hasta los 73 años (1) .
Es una neoplasia maligna de naturaleza mesenquimatosa, productora de sustancia intersticial y células que adoptan apariencia de cartílago hialino, con diversos grados de inmadurez y frecuentes focos de calcificación, que pueden presentarse en diferentes localizaciones.
Se pueden clasificar según su ubicación en: A- central , B- justo cortical (paraóstico o perióstico) (23,2,24,6,3) , C- periférico (o exofítico, que se presenta en la cubierta cartilaginosa de una osteocondroma) (28) y D- de tejidos blandos (13) ; en cuanto a histología : A- grado de anaplasia: clasificada en grados I, II y III, B- células desdiferenciadas, C- mesenquimales y D- células claras ; en cuanto a su origen, también pueden ser: 1 – primario y 2 – secundario (que se origina en el sitio de una lesión cartilaginosa benigna preexistente, como en la enfermedad de Ollier (encondromatosis) o el síndrome de Maffucci, es frecuente la transformación a condrosarcoma (20 al 30 %) (2,28), pudiendo ocurrir también como consecuencia de osteocondromas solitarios (en menos del 1%) o múltiples (10%) (2) y, más raramente, secundarios a la enfermedad de Paget.
El dolor puede ser un síntoma insidioso durante varios años, evolucionando con un crecimiento lento, aumento de volumen, movilidad restringida y la piel a veces enrojecida y caliente (23) . El primer síntoma suele ser una fractura ósea patológica (2,24) .
La radiografía muestra lesiones metafisarias radiotransparentes reemplazando la médula ósea que se extienden hasta la epífisis o diáfisis, erosionando la corteza interna (lesiones perforadoras), inflando o expandiendo la porción medular del hueso, pero quedándose delimitadas por la corteza engrosada.
Es frecuente la aparición de calcificaciones (moteadas, como copos de algodón (5) o en forma de anillos) (23, 2, 24, 13, 6, 28) . Éstas se deben a la degeneración del cartílago que recibe nueva vascularización y se calcifica. Este proceso se acelera en los condrosarcomas y se ralentiza en las lesiones cartilaginosas benignas y de bajo grado.
El mapeo óseo ayuda a estadificar la lesión y la resonancia magnética y la tomografía son importantes para evaluar la extensión intramedular y extraósea de la lesión (2) .
El diagnóstico del condrosarcoma bien diferenciado presenta dificultades histológicas y se deben valorar los datos de la historia clínica, localización y aspectos imagenológicos para la conclusión diagnóstica y definición del manejo adecuado (23, 14, 12) . Los detalles histológicos de irregularidad en la disposición y número de células dentro de la matriz condroide, cambios nucleares de hipercromasia, polimorfismo y mitosis atípicas, cuando se localizan en raíces de extremidades, deben considerarse condrosarcomas grado I, aunque estos mismos aspectos histológicos pueden encontrarse en benignos. Condromas de manos y pies. Bajo microscopía, las descripciones son similares a los condrosarcomas centrales (23) .
Para el diagnóstico también es necesario diferenciar las similitudes anatomopatológicas, clínicas y radiológicas con otras lesiones.
Diagnostica el quiste óseo aneurismático, por su carácter multiloculado; con condroma, osteocondroma, condroblastoma, osteosarcoma paraóstico y perióstico (con condrosarcoma yuxtacortical) (16) ; miositis osificante; fibroma condromixoide; TGC y linfoma no Hodgkin (23, 6, 28) . El condrosarcoma de células claras tiene formación intralesional de hueso reactivo, lo que puede causar confusión con el osteosarcoma. El condrosarcoma mesenquimatoso está formado por láminas de células pequeñas y redondeadas que se asemejan al hemangiopericitoma y al sarcoma de Ewing (14) . El condroma central de huesos largos, el condrosarcoma y el infarto óseo suelen ser de difícil diagnóstico, requiriendo periódicamente evaluación clínica y radiográfica para monitorear la evolución de la lesión y definir el manejo.
A menudo, la biopsia puede no ser definitiva para el diagnóstico (23, 28, 12) .
El tratamiento del condrosarcoma es exclusivamente quirúrgico (25) , debiendo optarse por una resección amplia, incluyendo el trayecto de la biopsia (21, 13) . La radioterapia es ineficaz (6) para controlar esta neoplasia. Para los casos de grado III, la indicación de quimioterapia se puede discutir con el protocolo utilizado para los sarcomas de células grandes de alto grado. En el condrosarcoma mesenquimatoso, que presenta predominio de células pequeñas indiferenciadas, la quimioterapia analizada se enmarca en el protocolo de tratamiento del sarcoma de Ewing. En ambos casos, la respuesta a la quimioterapia suele ser mala (6) . El tratamiento de esta neoplasia debe individualizarse para cada subtipo clínico.
A medida que ocurren complicaciones, las metástasis hematógenas a los pulmones (28) también pueden presentar diseminación linfática y recurrencia local. Muchos condrosarcomas tienen tendencia a invadir localmente (14) , alcanzando tamaños enormes, volviéndose inoperables y provocando la muerte por complicaciones de esta diseminación local.
La recurrencia local aumenta la incidencia de metástasis pulmonares (21) .
EJERCICIOS:
1. ¿Cuáles son las características radiográficas del condrosarcoma central?
- Osificación intra y extra medular.
- lesión diafisaria con rarefacción ósea y triángulo de Codman con reacción laminar gruesa.
- áreas de rarefacción ósea, erosión de la corteza interna y focos de calcificación.
- áreas de condensación ósea con reacción perióstica de piel de cebolla.
Respuesta : c) el tejido cartilaginoso es más radiopaco que el hueso y, por tanto, se presenta como una rarefacción ósea que provoca agrandamiento del hueso medular y lesiones en forma de saco en la corteza interna, provocando erosiones. Este tejido de cartílago reproductivo recibe brotes vasculares y el cartílago retrocede y se calcifica.
2. ¿Cuáles son las características de resonancia magnética del condrosarcoma?
- hiperseñal en T1, baja señal en T2 y con captación de contraste.
- hiposeñal en T1, hiposeñal en T2 y con captación de contraste.
- hiposeñal en T1, hiperseñal en T2 y sin captación de contraste.
- Señal baja en T1, señal alta en T2 y con captura de contraste.
Respuesta : d) el tejido cartilaginoso tiene señal baja e intermedia en T1. Intermedio por el cartílago y bajo por los focos de calcificación. Presenta captación de contraste por aumento del metabolismo local, por neoplasia.
3. ¿Cuáles son los principales diagnósticos diferenciales del condrosarcoma central?
- Infarto óseo y condroma.
- osteocondroma y sarcoma de Ewing
- osteomielitis y TGC
- osteosarcoma y condroblastoma.
Respuesta : a) el infarto óseo provoca una lesión de condensación en la médula ósea, pero no provoca erosión de la corteza interna y no presenta dolor progresivo. Suele ser un hallazgo diagnóstico en una radiografía ocasional. Lo mismo ocurre con el condroma que no evoluciona y representa únicamente restos cartilaginosos de desarrollo.
4. ¿Cuál es el tratamiento recomendado para el condrosarcoma central?
- Legrado intralesional e injerto óseo autólogo.
- Resección amplia y sustitución por endoprótesis no convencional.
- Legrado intralesional, adyuvante local con nitrógeno líquido e injerto óseo homólogo.
- Legrado intralesional, adyuvante local con electrotermia y cemento óseo.
Respuesta : b) la cirugía de resección amplia garantiza el tratamiento oncológico y la reconstrucción con endoprótesis proporciona la mejor restauración de la función.
5. Histológicamente resulta difícil realizar un diagnóstico diferencial entre:
- osteosarcoma y granuloma eosinofílico.
- Condrosarcoma y condroma grado I.
- TGC y sarcoma de Ewing.
- osteoblastoma y encondroma.
Respuesta : b) el condroma central de los huesos largos y el condrosarcoma de grado I suelen ser difíciles de diagnosticar histológicamente, requiriendo evaluación radiográfica para su definición y tratamiento.
Referencias bibliográficas
- ACKERMAN, LV; SPJUT, HJ Tumores de hueso y cartílago. Atlas de patología tumoral. Washington, Instituto de la Fuerza Aérea. Patología, 1962, fasc, 4.
- CANALE, ST Campbell Cirugía Ortopédica. Barueri: Manole; 2006
- DAHLIN, DC Tumores óseos. Barcelona: Ediciones Toray S/A; mil novecientos ochenta y dos
- DORFMAN, HD; CZERNIAK, B. Tumores óseos . St. Louis, CV Mosby Co., 1997, cap. 7, p.410.
- EDEIKEN, J.; HODES, PJ Diagnóstico radiológico de las enfermedades humanas. Buenos Aires, Panamericana, 1977, cap. 15.
- ETCHEBEHERE, M. Tumores cartilaginosos malignos: Condrosarcomas. En: Camargo OP Clínica Ortopédica. Río de Janeiro: Med si; 2002. pág. 753-759
- FELDMAN, F. Tumores cartilaginosos y afecciones similares a tumores formadores de cartílago de las cápsulas y los tejidos blandos. En: Enfermedades del sistema esquelético (diagnóstico por radiografía). Parte. 6 – Tumores óseos, Nueva York, Springer-Verlag, 1977, p.177.
- FLETCHER, CDM, Unni KK, OMS – Merters F. (Eds.): Organización Mundial de la Salud. Clasificación de Tumores. Patología y Genética de Tumores de Tejidos Blandos y Huesos. Prensa IARC: Lyon 2002.
- GREENSPAN, A. Radiología ortopédica. Río de Janeiro: Guanabara; 2001.
- HENDERSON, ED; Le PAGE, GA Apud FELDAMAN, F. Tumores de cartilaginio y cartílago que forman afecciones similares a tumores del hueso y los tejidos blandos. En: Enfermedad del sistema esquelético (diagnóstico por radiografía). Parte. 6 – Tumores óseos, Nueva York, Springer Verlag, 1977, p.182.
- HUVOS, AG Tumores óseos Diagnóstico , Tratamiento y Pronóstico . Filadelfia, WB Saunders Co., 1979, pág. 13.
- JAFFE, HL Tumores y estados tumorales de huesos y articulaciones. México: La Prensa Médica Mexicana; 1966.
- JESÚS-GARCIA, R. – Reynaldo Jesús-García
- LICHTENSTEIN, L. Barcelona: Talleres Gráficos Iberoamericanos; 1975.
- LICHTESTEIN, L. Tumor óseo . 4 Ed St. Louis, CV Mosby Co., 1972, cap. 15.
- LICHTESTEIN, L.; BERNSTEIN, D. Tumores condroides óseos benignos y malignos inusuales. Cáncer , 12:1142, 1959.
- MARCOVE, RC Condrosarcoma: Diagnóstico y tratamiento. En: Clínicas Ortopédicas de América del Norte. Tumores del aparato musculoesquelético . Buenos Aires, Panamericana, 1977, cap. 7.
- MARCOVE, RC et al. Condrosarcoma de pelvis y extremo superior del fémur. En el análisis de los factores que influyen en el tiempo de supervivencia en 113 casos. J. Bone Joint Surg., 54A:61, 1972.
- MARCOVE, RC; SHOJI, H.; HARLEN, M. Metabolismo alterado de carbohidratos en tumores cartilaginosos. Contemporáneo. Cirugía . 5:53, 1974.
- McFARLAND, GBJr.; McKINLEY, LM; REED, RJ Desdiferenciación de condrosarcomas de bajo grado. Clínica. Ortopédico. , 122:157, 1971.
- MENÉNDEZ, LR Actualización de conocimientos en ortopedia: Actualizaciones en cirugía ortopédica y traumatología. Barcelona: Ars Médica; 2003.
- O’NEAL, LW; ACKERMAN, LV Condrosarcoma de cap. Cáncer , 5:551, 1952.
- PROSPERO, JD Tumores óseos. São Paulo, Roca, 2001, cap. II.
- ROBINOS. Patología estructural y funcional. Río de Janeiro: Guanabara; 1996.
- ROMSDAHL, M.; EVANS, HL; AYALA, AG Tratamiento quirúrgico del condrosarcoma. En: Manejo de tumores primarios de huesos y tejidos blandos . Chicago, Anuario médico. Editor Inc., 1977, pág. 125.
- SCHAJOWICZ, F. Tumores y Lesiones Seudotumorales de Huesos y Articulaciones. Buenos Aires: Editora Médica Panamericana; mil novecientos ochenta y dos.
- TORNBERG, DN; ARROZ, RW; JOHNSTON, AD La ultraestructura del fibroma condromixoide. Clínica. Ortopédico. Investigación relativa , 95:295, 1973.
Autores del caso
Autor: Profr. Dr. Pedro Péricles Ribeiro Baptista
Oncocirugía Ortopédica en el Instituto Oncológico Dr. Arnaldo Vieira de Carvalho
Oficina : Rua General Jardim, 846 – Cj 41 – Cep: 01223-010 Higienópolis São Paulo – SP
Teléfono: +55 11 3231-4638 Celular:+55 11 99863-5577 Correo electrónico: drpprb@gmail.com